Ha habido alguna discordancia sobre quién merece ser reconocido como creador de la tabla periódica, si el alemán Lothar Meyer o el ruso Dmitri Mendeleiev.
En 1868, Meyer construyó una tabla extendida que entregó a un colega para su evaluación. Desgraciadamente para Meyer, la tabla de Mendeleiev se publicó en 1869, un año antes de que apareciera la de Meyer.
Dmitri Ivanovich Mendeleiev (1834-1907), el menor de 17 hermanos, nació en el pueblo Siberiano de Tobolsk donde su padre era profesor de literatura rusa y filosofía.
1864 En el momento que Mendeleiev desarrolló su tabla periódica, las masas atómicas experimentalmente determinadas no siempre eran exactas, y reordenó de nuevo los elementos a pesar de sus masas aceptadas. Por ejemplo, cambió el peso del berilio de 14 a 9. Esto colocó al berilio en el Grupo 2 encima del magnesio cuyas propiedades se parecían más que donde se había colocado antes (encima del nitrógeno).
GRUPO PERIODO Y BLOQUE.
ESTON SON LOS GRUPOS DE LA TABLA PERIODICA
Grupo 1 (I A): los metales alcalinos
Grupo 2 (II A): los metales alcanetorrios
Grupo 3 (III B): Familia del escandio
Grupo 4 (IV B): Familia del titanio
Grupo 5 (V B): Familia del vanadio
Grupo 6 (VI B): Familia del cromo
Grupo 7 (VII B): Familia del magnadeso
Grupo 8 (VIII B): Familia del hierro
Grupo 9 (VIII B): Familia del cobalto
Grupo 10 (VIII B): Familia del Níquel
Grupo 11 (I B): Familia del cobre
Grupo 12 (II B): Familia del zinc
Grupo 13 (III A): los terreos
Grupo 14 (IV A): los carbonoideos
Grupo 15 (V A): los nitrogeneidos
Grupo 16 (VI A): los calcógenos o anfigeneos
Grupo 17 (VII A): los halogenos
Grupo 18 (VIII A): los gases nobles
LOS PERIODOS SON:
La tabla periódica consta de 7 períodos:
La tabla también está dividida en cuatro grupos, s, p, d, f, que están ubicados en el orden sdp, de izquierda a derecha, y actinidos
Tabla periódica dividida en bloques
La tabla periódica se puede también dividir en bloques de elementos según el orbital que estén ocupando los electrones más externos.
Los bloques o regiones se denominan según la letra que hace referencia al orbital más externo: s, p, d y f. Podría haber más elementos que llenarían otros orbitales, pero no se han sintetizado o descubierto; en este caso se continúa con el orden alfabético para nombrarlos.
bloque:S
bloque:P
bloque:D
bloque:F
PROPIEDADES PERIODICAS
La electronegatividad de un elemento mide su tendencia a atraer hacia sí electrones, cuando está químicamente combinado con otro átomo. Cuanto mayor sea, mayor será su capacidad para atraerlos.
Pauling la definió como la capacidad de un átomo en una molécula para atraer electrones hacia así. Sus valores, basados en datos termoquímicos, han sido determinados en una escala arbitraria, denominada escala de Pauling, cuyo valor máximo es 4 que es el valor asignado al flúor, el elemento más electronegativo.
ENERGIA DE IONIZACION.
La energía de ionización, potencial de ionización o EI es la energía necesaria para separar un electron en su estado fundamental de un atomo, de un elemento en estado de gas La reacción puede expresarse de la siguiente forma:
 .
.
Siendo 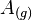 los átomos en estado gaseoso de un determinado elemento quimico;
los átomos en estado gaseoso de un determinado elemento quimico;  , la energía de ionización y
, la energía de ionización y  un electron.
un electron.
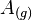 los átomos en estado gaseoso de un determinado elemento quimico;
los átomos en estado gaseoso de un determinado elemento quimico;  , la energía de ionización y
, la energía de ionización y  un electron.
un electron.
AFINIDAD ELECTRONICA.
La afinidad electrónica (AE) o electroafinidad se define como la energia liberada cuando un atomo gaseoo neutro en su estado fundamental (en su menor nivel de energía) captura un electron y forma un ion mononegativo:
Dado que se trata de energía liberada, pues normalmente al insertar un electrón en un átomo predomina la fuerza atractiva del nucleo, tiene signo negativo. En los casos en los que la energía sea absorbida, cuando ganan las fuerzas de repulsión, tendrán signo positivo; AE se expresa comúnmente en el sistema internacional en kJ·mol-1.
RADIO Y VOLUMEN ATOMICO.
RADIO: Identifica la distancia que existe entre el nucleo y el orbital más externo de un atomo. Por medio del radio atómico, es posible determinar el tamaño del átomo.
VOLUMEN:Identifica la distancia que existe entre el nucleo y el orbital más externo de un atomo. Por medio del radio atómico, es posible determinar el tamaño del átomo.
Volumen del átomo = masa atómica / densidad.
UTILIDAD EH IMPORTANCIA DE LOS METALES Y NO METALES PARA LA VIDASOCIECONOMICA DEL PAIS.
Metales
La mayor parte de los elementos metálicos exhibe el lustre brillante que asociamos a los metales. Los metales conducen el calor y la electricidad son maleables (se pueden golpear para formar láminas delgadas) y dúctiles (se pueden estirar para formar alambres). Todos son sólidos a temeratura ambente con ecepcion a mercurio (punto de fuision=-39 ºC), que es un líquido. Dos metales se funden ligeramente arriba de la temperatura ambiente: el cesio a 28.4 ºC y el galio a 29.8 ºC. En el otro extremo, muchos metales se funden a temperaturas muy altas. Por ejemplo, el cromo se funde a 1900 ºC.
NO METALES
Los no metales varían mucho en su apariencia no son lustrosos y por lo general son malos conductores del calor y la electricidad. Sus puntos de fusión son más bajos que los de los metales (aunque el diamante, una forma de carbono, se funde a 3570 ºC). Varios no metales existen en condiciones ordinarias como moléculas diatómicas.
Metales
|
no metales
|
Tienen un lustre brillante; diversos colores, pero casi todos son plateados.
Los sólidos son maleables y dúctiles
Buenos conductores del calor y la electricidad
Casi todos los óxidos metálicos son sólidos iónicos básicos.
Tienden a formar cationes en solución acuosa.
Las capas externas contienen poco electrones habitualmente trss o menos.
|
No tienen lustre; diversos colores.
Los sólidos suelen ser quebradizos; algunos duros y otros blandos.
Malos conductores del calor y la electricidad
La mayor parte de los óxidos no metálicos son sustancias moleculares que forman soluciones ácidas
Tienden a formar aniones u oxianiones en solución acuosa.
Las capas externas contienen cuatro o más electr
|
En la vida cotidiana tenemos una gran cantidad de Herramientas, Tecnologías y Utensilios que utilizan en mayor o menor medida a los Metales como parte de su conformación, como sostén a las distintas estructuras, como también para poder brindar una utilidad a su funcionamiento, siendo muy importante su extracción y utilización, mucho más de lo que pensamos.
Después del cobre, se descubrieron nuevas aleaciones del cobre como el estaño o el plomo, que juntos dieron lugar a un nuevo producto, el bronce; este nuevo material es menos maleable, pero más duro. Un gran salto tecnológico se dio con el uso de la forja, estos hornos de alta temperatura hicieron posible la manipulación del hierro para producir herramientas aún más resistentes. Esta secuencia tecnológica ha configurado la denominación de las diferentes etapas de la edad de los metales: la edad del cobre, la edad del bronce, la edad del hierro.











No hay comentarios.:
Publicar un comentario