| Año | Científico | Descubrimientos experimentales | Modelo atómico | ||||||
| 1808 |  John Dalton |
|
| ||||||
| 1897 |  J.J. Thomson |
|
| ||||||
| 1911 |  E. Rutherford |
|
| ||||||
| 1913 |  Niels Bohr |
|
| ||||||
APORTACIONES AL MODELO ATOMICO ACTUAL REALIZADAS.
DALTON.
LA REGLA DE HUND: cuando hay varios electrones ocupando orbitales degenerados, de igual energía, lo harán en orbitales distintos y con espines paralelos, siempre que esto sea posible.
El modelo atómico de Dalton1 surgido en el contexto de la química, fue el primer modelo atómico con bases científicas, propuesto entre 1803 y 1807 por john dalton aunque el autor lo denominó más propiamente "teoría atómica" o "postulados atómicos".
El modelo permitió aclarar por primera vez por qué las sustancias químicas reaccionaban en proporciones esteqiometricas fijas (ley de las proporciones constantes), y por qué cuando dos sustancias reaccionan para formar dos o más compuestos diferentes, entonces las proporciones de estas relaciones son números enteros (ley de las proporciones multlipes). Por ejemplo 12 g de carbono (C), pueden reaccionar con 16 g de oxígeno (O2) para formar monoxcido (CO) o pueden reaccionar con 32 g de oxígeno para formar dioxido de carbono (CO2). Además el modelo aclaraba que aún existiendo una gran variedad de sustancias diferentes, estas podían ser explicadas en términos de una cantidad más bien pequeña de constituyentes elementales o elementos. En esencia, el modelo explicaba la mayor parte de la química de fines de siglo XVIII reduciendo una serie de hechos complejos a una teoría combinatoria realmente simple.
THOMSON.
Thomson es una teoría sobre la estructura atomica propuesta en 1904 por joseph john tomson quien descubrió el electron en 1897, mucho antes del descubrimiento del proton y del neutron. En dicho modelo, el atomo está compuesto por electones de carga negativa en un átomo positivo, incrustados en este al igual que las pasas de un pudin. A partir de esta comparación, fue que el supuesto se denominó «Modelo del pudin de pasas».Postulaba que los electrones se distribuían uniformemente en el interior del átomo suspendidos en una nube de carga positiva. El átomo se consideraba como una esfera con carga positiva con electrones repartidos como pequeños gránulos. La herramienta principal con la que contó Thomson para su modelo atómico fue la electricidad.
RUTHERFORD.
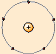
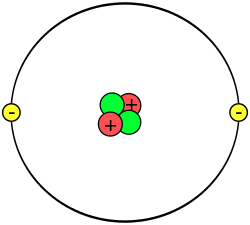
El modelo atómico de Rutherford1 es un modelo atomico o teoría sobre la estructura interna del atomo propuesto por el químico y físico británico-neozelandés erenest rutherfold para explicar los resultados de su experimento de la lamina de oro, realizado en 1911.
El modelo de Rutherford fue el primer modelo atómico que consideró al átomo formado por dos partes: la "corteza" (luego denominada periferia), constituida por todos sus electrones, girando a gran velocidad alrededor de un "núcleo" muy pequeño; que concentra toda la carga eléctrica positiva y casi toda la masa del átomo.
CONSEPTOS DEL NUMERO ATOMICO
CONSEPTOS DEL NUMERO ATOMICO
es la porción más pequeña de cualquier elemento químico, que no puede dividirse y que dispone de existencia independiente. Los átomos están compuestos por electrones que orbitan en torno a un núcleo con neutrones y protones. El número atómico indica el número de protones en el núcleo de un átomo. El número atómico es un concepto importante de la química y de la mecánica cuántica.El elemento y el lugar que éste ocupa en la tabla periódica derivan de este concepto. Cuando un átomo es generalmente eléctricamente neutro, el número atómico será igual al número de electrones del átomo que se pueden encontrar alrededor de la corteza. Estos electrones determinan principalmente el comportamiento químico de un átomo. Los átomos que tienen carga eléctrica se llaman iones. Los iones pueden tener un número de electrones más grande. Los átomos de diferentes elementos presentan distintas cantidades de protones.
SIGNIFICADOS Y VALORES DE LOS NUMEROS CUANTICOS.
Los números cuánticos son valores numéricos que nos indican las características de los electrones de los átomos. Están basados, desde luego, en la teoría atómica de Neils Bohr que es el modelo atómico más aceptado y utilizado en los últimos tiempos.
ESTOS SON LOS NUMEROS CUANTICOS MAS IMPORTANTES .
- Número Cuántico Principal.
- Número Cuántico Secundario.
- Número Cuántico Magnético.
- Número Cuántico de Spin.
Número Cuántico de Spin (s): El número cuántico de spinnos indica el sentido de rotación en el propio eje de los electrones en un orbital
REGLAS PARA ELABORAR LAS CONFIGURACONES ELECTRONICAS.
e conoce como configuración electrónica de un átomo, a la distribución de los electrones de un átomo en orbitales. Cuando la configuración electrónica es la de menor energía, se conoce como configuración electrónica fundamental.
LA CONFIGURACION ELECTRONICA SE CONSIGUE A PARTIR DE TRES REGLAS
REGLA DE CONSTRUCCION: se consigue colocando a los electrones uno a uno en los distintos orbitales disponibles para el átomo, que se disponen en orden creciente de energía.
REGLA DE PAUILI: dice que:
Dos electrones de un mismo átomo, no pueden poseer sus cuatro números cuánticos iguales, Debido a que cada orbital está definido por los números cuánticos n, l, y m, solamente hay dos posibilidades ms = -1/2 y ms = +1/2, que refleja físicamente que cada orbital puede contener un máximo de dos electrones,
LA REGLA DE HUND: cuando hay varios electrones ocupando orbitales degenerados, de igual energía, lo harán en orbitales distintos y con espines paralelos, siempre que esto sea posible.
APLICACIONES DE LOS ISOTOPOS RAIACTIVOS.
Los isotopos son atomos de un mismo elemento con igual numero atomico (Z)y diferentes numeros de masa (A) debido a diferentes numero de neutrones.
POR EJEMPLO:LOS ISOTOPOS DE HIDROGENO SON 3
1
H
1
protio
un proton
un electron
2
H
1
deuterio
un proton
un neutron
un electron
3
H
1
tritio
un proton
dos neutrones
un electron
aunque un elemento cuente con isotopos todos sus atomos se comportan de la misma manera debido al numero de electones .
Cada uno de los distintos tipos de átomos tienen sus isotopos, incluso un mismo átomo puede tener muchos tipos de isótopos, algunos de ellos son estables pero otros, como es el caso del uranio, son bastante inestables por lo que el átomo emite radiación de forma espontánea mientras se convierte en un átomo más estable lo cual hace que se denomine isotopo radioactivo











No hay comentarios.:
Publicar un comentario