ENLACE QUIMICO
Un enlace químico es la interaccion fisica responsable de las interacciones entre atomos, moleculas e iones, que tiene una estabilidad en los compuestos diatomicos y poliatómicos.
En general, el enlace químico fuerte está asociado en la transferencia de electrones de valencia entre los átomos participantes. Las moléculas, cristales, y gases diatómicos (que forman la mayor parte del ambiente físico que nos rodea) está unido por enlaces químicos, que determinan las propiedades físicas y químicas de la materia.
Las cargas opuestas se atraen, porque, al estar unidas, adquieren una situación más estable que cuando estaban separados. Esta situación de mayor estabilidad suele darse cuando el número de electrones que poseen los átomos en su último nivel es igual a ocho, estructura que coincide con la de los gases nobles ya que los electrones que orbitan el núcleo están cargados negativamente, y que los protones en el núcleo lo están positivamente, la configuración más estable del núcleo y los electrones es una en la que los electrones pasan la mayor parte del tiempo entre los núcleos, que en otro lugar del espacio. Estos electrones hacen que los núcleos se atraigan mutuamente.
REGLA DE OCTETO.
La regla del octeto, enunciada en 1916 por Gilbert Newton Lewis, Físicoquímico norteamericano, dice que la tendencia de los iones de los elementos del sistema periódico es completar sus últimos niveles de energía con una cantidad de 8electrones, de tal forma que adquiere una configuración muy estable. Esta configuración es semejante a la de un gas noble,1 los elementos ubicados al extremo derecho de la tabla periódica. Los gases nobles son elementos electroquímicamente estables, ya que cumplen con la estructura de Lewis, son inertes, es decir que es muy difícil que reaccionen con algún otro elemento. Esta regla es aplicable para la creación de enlaces entre los átomos, la naturaleza de estos enlaces determinará el comportamiento y las propiedades de las moléculas. Estas propiedades dependerán por tanto del tipo de enlace, del número de enlaces por átomo, y de las fuerzas intermoleculares.
ENLACE IONICOY SUS PROPIEDADES
En quimica, un enlace iónico o electrovalente es la unión de atomos que resulta de la presencia de atracción electrotastica entre los iones de distinto signo, es decir, uno fuertemente electropositivo (baja energia ionizacion) y otro fuertemente electronegativo Eso se da cuando en el enlace, uno de los atomos capta electrones del otro. La atracción electrostática entre los iones de carga opuesta causa que se unan y formen un compuesto químico simple, aquí no se fusionan; sino que uno da y otro recibe. Para que un enlace iónico se genere es necesario que la diferencia (delta) de electronegatividades sea más que 1.7
Cabe resaltar que ningún enlace es totalmente iónico, siempre habrá una contribución en el enlace que se le pueda atribuir a la compartición de los electrones en el mismo enlace (covalencia). El modelo del enlace iónico es una exageración que resulta conveniente ya que muchos datos termodinámicos se pueden obtener con muy buena precisión si se piensa que los átomos son iones y no hay compartición de electrones.
ELACE COVALENTE
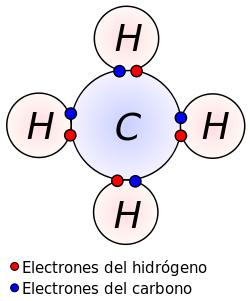
Un enlace covalente entre dos átomos se produce cuando estos átomos se unen, para alcanzar el octeto estable, compartiendo electrones del último nivel1(excepto el hidrogeno que alcanza la estabilidad cuando tiene 2 electrones). La diferencia de electronegatividad entre los átomos no es lo suficientemente grande como para que se produzca una unión de tipo iónica. Para que un enlace covalente se genere es necesario que la diferencia de electronegatividad entre átomos sea menor a 1,7.
De esta forma, los dos átomos comparten uno o más pares eletronicos en un nuevo tipo de orbital, denominado orbital molecular. Los enlaces covalentes se producen entre átomos de un mismo elemento no metal y entre distintos elementos no metales.
CARACTERISTICAS DE LO DIFERENTES TIPOS DE ENLACE COVALENTE
Un enlace covalente entre dos átomos se produce cuando estos átomos se unen, para alcanzar el octeto estable, compartiendo electrones del último nivel. La diferencia de electronegatividad entre los átomos no es lo suficientemente grande como para que se produzca una unión de tipo iónica. Para que un enlace covalente se genere es necesario que la diferencia de electronegatividad entre átomos sea menor a 1,7.
De esta forma, los dos átomos comparten uno o más pares electronicos en un nuevo tipo de orbital, denominado orbital molecular. Los enlaces covalentes se producen entre átomos de un mismo elemento no metal y entre distintos elementos no metales.Cuando átomos distintos de no metales se unen una forma covalente, uno de ellos resultará más electronegativo que el otro, por lo que tenderá a atraer la nube electronica su núcleo, generando un dipolo eléctrico. Esta polarización permite que las moléculas del mismo compuesto se atraigan entre sí por fuerzas electrostáticas de distinta intensidad
Covalente apolar
Conocido además por enlace covalente puro , o covalente no polar. Se produce por el compartimiento de electrones entre dos o más átomos de igual electronegatividad por lo que su resultado es 0, y por tanto la distribución de carga electrónica entre los núcleos es totalmente simétrica, por lo que el par electrónico es atraído igualmente por ambos núcleos.
H• + •H = H:H o bien H- H
COBALENTE POLAR:Es una transición entre el enlase ionico puro y el enlace covalente apolar. Se produce por el compartimiento de electrones entre dos o más átomos de diferentes electronegatividad, estableciéndose una separación de cargas (que simbolizaremos como d+y d-) o lo que es igual, la distribución de carga electrónica entre los núcleos será asimétrica, pero esta diferencia no llega al punto en que el enlace se torna iónico puro. Son posibles diferentes grados de polaridad del enlace.
Covalente coordinado o dativo
Se produce cuando dos átomos comparten una pareja de electrones, pero dicha pareja procede solamente de uno de los átomos combinados.
El átomo que aporta la pareja de electrones recibe el nombre de donante, y el que los recibe, aceptor. Cuando queremos simplificar la fórmula electrónica se pone una flecha (→) que va del donante al aceptor.
PROPIEDADES DE LOS COMPUESTOS COVALENTES
Las sustancias con enlaces covalentes forman en general dos clases de compuestos: los cristales covalentes y sustancias moleculares . Los cristales covalentes o atómicos, están constituidos por redes de enlaces covalentes que se extienden sin solución de continuidad en las tres direcciones del espacio terminando donde termina el cristal.
Las sustancias moleculares están formadas por moléculas discretas de mayor o menor tamaño, unidas entre sí por fuerzas intermoleculares
Existen también sustancias covalentes con estructuras especiales que no se pueden encuadrar en ninguno de lo tipos establecidos.
TEORIAS QUE EXPLICAN EL ENLACE METALICO (TEORIA DELMAR DE ELECTRONES Y LA TEORIA DE BANDAS.
El enlace metálico es muy distinto a los dos tipos de enlaces que hemos visto hasta ahora: el enlase covalentes y el enlace ionico. En los compuestos metálicos los átomos están muy próximos los unos a los otros y forman estructuras compactas. Además, presentan unas características propias, entre las que destaca la elevada conductividad eléctrica. Esta propiedad, la de la conductividad, requiere para ser explicada que los electrones implicados en el enlace metálico tengan libertad y facilidad de movimiento. Es por este motivo que, para que los metales tengan electrones móviles, requieren 2 características a nivel atómico: la primera, una energía de ionización baja (recordemos que la energia de ionizacion es la energía necesaria para arrancar un electrón de la capa de valencia) y la segunda, que posean orbitales de valencia vacíos y accesibles que permitan a los electrones moverse con facilidad.
Cualquier teoría sobre el enlace metálico debe dar explicación a esta libertad de movimiento electrónico y a las restantes propiedades de los metales. Estas son dos: la llamada teoría del gas
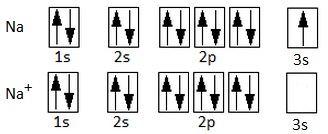
En la teoría del gas electrónico (también llamada del mar de electrones o de la nube electrónica), los átomos metálicos pierden sus electrones de valencia y forman una red compacta de cationes. Por ejemplo, en el caso del sodio, cuya configuración electrónica es:
CARACTERISTICAS QUE SE DERIVAN DEL ENLACE METALICO.
Teoría del mar de electrones
Teoría de bandas
Los metales tienen ciertas características, las cuales son:
FUERZAS INTERMOLECULARES.
se definen como el conjunto de fuerzas atractivas y repulsivas que se producen entre las moléculas como consecuencia de la presencia o ausencia de electrones.
Cuando dos o más átomos se unen mediante un enlace químico forman una molécula, los electrones que conforman la nueva molécula recorren y se concentran en la zona del átomo con mayor electronegatividad, definimos la electronegatividad como la propiedad que tienen los átomos en atraer electrones. La concentración de electrones en una zona específica de la molécula crea una carga negativa, mientras que la ausencia de los electrones crea una carga positiva.
Denominamos dipolos a las moléculas que disponen de zonas cargadas negativamente y positivamente debido a la electronegatividad y concentración de los electrones en las moléculas.
Podemos asimilar el funcionamiento de un dipolo a un imán con su polo positivo y su polo negativo, de tal forma que si acercamos otro imán el polo positivo atraerá al polo negativo y viceversa, dando como resultado una unión.
CARACTERISTICAS DE LOS COMPUESTOS QUE PRESENTAN UN PUENTE DE HIDROGENO ESPECIALMENTE LA DEL AGUA Y MOLECULAS DE IMPORTANCIA BIOLOGICA.
LOS PUENTES DE HIDROGENO
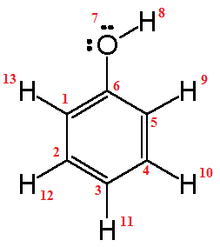
El puente de hidrógeno es un enlace que se establece entre moléculas capaces de generar cargas parciales. El agua, es la sustancia en donde los puentes de hidrógeno son más efectivos, en su molécula, los electrones que intervienen en sus enlaces, están más cerca del oxígeno que de los hidrógenos y por esto se generan dos cargas parciales negativas en el extremo donde está el oxígeno y dos cargas parciales positivas en el extremo donde se encuentran los hidrógenos. La presencia de cargas parciales positivas y negativas hace que las moléculas de agua se comporten como imanes en los que las partes con carga parcial positiva atraen a las partes con cargas parciales negativas. De tal suerte que una sola molécula de agua puede unirse a otras 4 moléculas de agua a través de 4 puentes de hidrógeno. Esta característica es la que hace al agua un líquido muy especial.
PUENTES DE HIDROGENO EN EL AGUA
Los puentes de Hidrógeno, se forman por átomos de Hidrógeno localizados entre átomos electronegativos. Cuando un átomo de Hidrógeno está unido covalentemente, a una átomo electronegativo, ej. Oxígeno o Nitrógeno, asume una densidad (d) de carga positiva, debido a la elevada electronegatividad del átomo vecino. Esta deficiencia parcial en electrones, hace a los átomos de Hidrógeno susceptibles de atracción por los electrones no compartidos en los átomos de Oxígeno o Nitrógeno
Obsérvese la configuración electrónica del Oxígeno:
8O 1s2 2s2 2pxêé pyé pzé
de ahí que :
:
d+ d+
Figura: configuración electrónica del Oxígeno
el puente de Hidrógeno es relativamente débil entre -20 y -30 kJ mol-1, la fuerza de enlace aumenta al aumentar la electronegatividad y disminuye con el tamaño de los átomos participantes. Por tanto, el puente de Hidrógeno existe en numerosas moléculas no solo en el agua. Aquí solo se tratará lo referente al agua.
La estructura del agua favorece las interacciones para formar puentes de Hidrógeno, el arreglo siempre es perpendicular entre las moléculas participantes, además, es favorecido por que cada protón unido a un Oxígeno muy electronegativo encuentra un electrón no compartido con el que interactúa uno a uno. De lo anterior se concluye que cada átomo d Oxígeno en el agua interacciona con 4 protones, dos de ellos unidos covalentemente y dos a través de puentes de Hidrógeno.
colineales
COMPOSICIÒN QUÌMICA DEL AGUA
AGUA
PROPIEDADES BILOGICAS DEL AGUA
GRUPOS FUNCIONALES
CLASIFICACIÒN
MOLÉCULAS DE IMPORTANCIA BIOLÓGICA
Maryuri Beltran
Camila Ovalles
Camila Calderon
las proteinas sirven para la conformacion de moleculas en la membrana en su parte extracelular e intracelular, ademas de crear musculo a partir de los aminoacidos, tambien sirven para dar una orden a una celula, incluso para la replicacion de un virus, pero fundamentalmente son las que crean el organismo vivo como tal, en su sintesis en los ribosomas
los carbohidratos estos se descomponen hasta llegar a glucosa la cual va a ser aprovechada para formar acetil colina y asi poder entrar al ciclo de krebs, la glucosa que no hace eso y que sobra pasa al higado en forma de glucogeno en los seres superiores y en plantas en forma de almidon, es decir cadenas ramificadas de glucosa en uniones 1,4 lineal y 1,6 ramificadas.
las grasas conformacionalmente se utilizan para la formacion de nuevas celulas y tambien para el desempeño calorico, despues de los carbohidratos, es decir el colesterol es usado para que la celula tenga consistencia y las celulas no sean como masas gelatinosas, sino que tengan consistencia para poderse mover libremente.